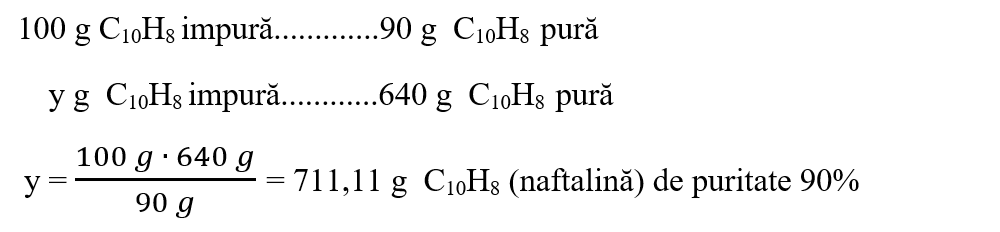II.5.6. Exerciții și probleme rezolvate la arene.
🔓 Exerciții și probleme rezolvate la arene
1. Denumește următoarele hidrocarburi aromatice:
a)

b)

c)

d)

e)

f)

Rezolvare:
- Cei 6 atomi de H din nucleul benzenic sunt identici. Dacă se înlocuiește un singur atom de H din ciclul benzenic se obține un singur derivat monosubstituit al benzenului
- În cazul derivaților disubstituiți ai benzenului, poziția substituenților se notează prin cifre sau folosind prefixele orto (o- pentru 1,2-dialchilbenzen), meta (m- pentru 1,3- dialchilbenzen) și para (p- pentru 1,4- dialchilbenzen).
- În cazul naftalinei, cele 8 grupe –CH- nu sunt toate echivalente între ele. Sunt echivalente numai pozițiile 1,4,5,8 care se notează cu α, precum și pozițiile 2,3,6,7 care se notează cu β. Deci naftalina poate avea numai doi derivați monosubstituiți: α și β.

- Radicalii proveniți de la arene se numesc aril, Ar-.
Exemple:
- Radicalul provenit de la benzen se numește fenil, C6H5-
- Radicalul provenit de la toluen se numește benzil, C6H5-CH2-
- Radicalul provenit de la naftalină se numește naftil, C10H7-
a)

b)

c)

d)

e)

f)

2. Scrie formulele structurale ale următorilor compuși aromatici:
a) Difenil
b) 1,4-dimetilbenzen (para-xilen)
c) Izopropilbenzen (cumen)
d) 1-nitronaftalină (α-nitronaftalină)
e) Acid benzensulfonic
f) 1,2,3,4-tetracloronaftalină
g) 2,4,6-trinitrotoluen (TNT)
h) Clorură de benzil
Rezolvare:
a)

b)

c)

d)

e)

f)

g)

h)

3. O hidrocarbură aromatică polinucleară, A, cu masa molară 128 g/mol conține 93,75 % C.
a) Determină formula moleculară și structurală a arenei A.
b) Scrie reacția de nitrare a ei.
c) Ce masă de arena A de puritate 90% este necesară pentru a obține 865 g de derivat al hidrocarburii A?
Rezolvare:
a)
Scriem datele problemei
μA = 128 g/mol
93,75 % C
Calculăm procentul de H
% H = 100 - 93,75 = 6,25 % H
Împărțim fiecare procent la masa elementului și apoi fiecare rezultat la cel mai mic număr:

Scriem formula brută: (C1,25H1)n și calculăm pe n cu masa molară:
n ∙ 12 ∙ 1,25 + n ∙ 1 ∙ 1 = 128
n ∙ 15 + n = 128
n ∙ 16 = 128
n = 8
Arena are formula moleculară: C10H8. Deci, este naftalina.
Formula structurală a naftalinei este:

b)
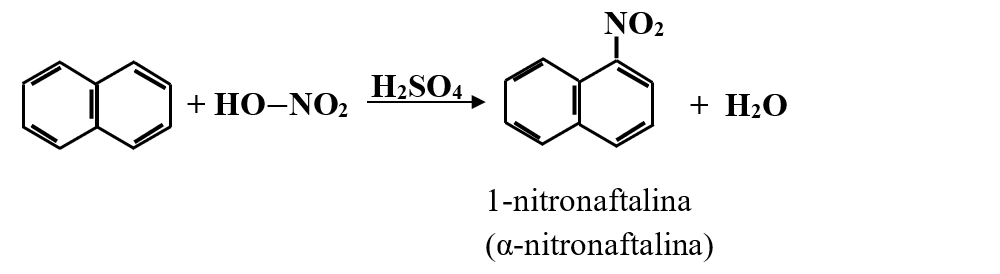
c)
Calculăm masa molară a α-nitronaftalinei (C10 H7 NO2):
μC10 H7 NO2 = 10 ∙ AC + 7 ∙ AH + 1 ∙ AN + 2 ∙ AO = 10 ∙ 12 + 7 ∙ 1 + 1 ∙ 14 + 2 ∙ 16
μC10 H7 NO2= 173 g/mol
Din ecuația reacției aflăm masa de naftalină pură care a dus la obținerea a 865 g de α-nitronaftalina (C10 H7 NO2):
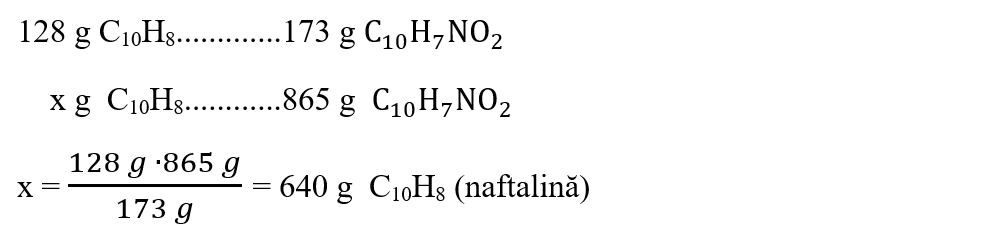
Aflăm masa naftalinei impure cu puritatea de 90% corespunzătoare unei mase de 640 g naftalină pură: