VII.4. Amfoliți acido-bazici. Caracter amfoter.
Apa poate funcţiona fie ca acid, donând un proton şi transformându-se în ion hidroxil, fie ca bază, acceptând un proton şi transformându-se în ion hidroniu.
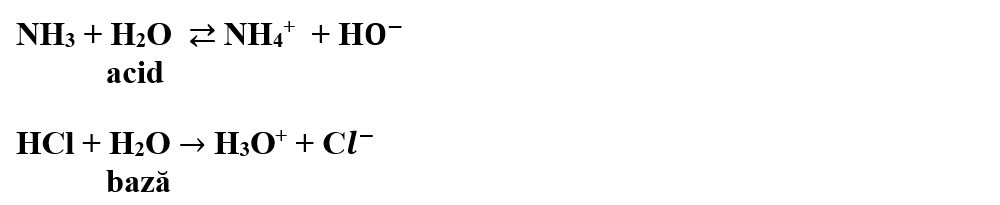
Substanțele care se comportă atât ca acid, cât și ca bază, în funcție de natura mediului, se numesc amfoliți acido-bazici.
Exemple de amfoliți acido-bazici:
- Apa este un amfolit acido-bazic
- Anionii acizi : HS-, HSO4-, HCO3-, H2PO4-, HPO4-2 etc.
De exemplu, ionul hidrogenosulfat este un amfolit acido-bazic:

- Unii hidroxizi precum Al(OH)3, Zn(OH)2 reacționează și cu acizi și cu baze.
Oxidul și hidroxidul de zinc au proprietăți amfotere, reacționând atât cu acizii, cât și cu bazele.
Hidroxidul de zinc în reacție cu acidul clorhidric formează clorură de zinc și apă:
Zn(OH)2 + 2HCl = ZnCl2 + 2H2O
Hidroxidul de zinc în reacție cu hidroxidul de sodiu formează un complex solubil în apă de tetrahidroxozincat de sodiu, Na2[Zn(OH)4]:
Zn(OH)2 + 2NaOH = Na2[Zn(OH)4]