VI.2.3. Identificarea și separarea cationilor din grupa a III a analitică.
Elementele din aceasta grupă, precipită, cu ionul sulfură, în mediu neutru sau alcalin.
Reactivul de grupă este sulfura de amoniu, (NH4)2S, iar precipitarea se face în prezența de hidroxid de amoniu. Sulfura de amoniu, nu precipită în mediu acid, dar în mediu bazic și la fierbere o parte din elementele acestei grupe precipită sub formă de sulfuri, iar altele sub formă de hidroxizi, datorită hidrolizei acestor sulfuri în mediu apos.
Cationii care fac parte din aceasta grupa sunt : Fe2+, Al3+, Cr3+, Fe3+, Ni2+, Zn2+, Mn2+, Co2+.
În funcție de modul cum precipită, cationii acestei grupe analitice se împart în două subgrupe, astfel :
a) Subgrupa cationilor trivalenți: Fe3+, Al3+, Cr3+
Acești cationi formează cu (NH4)2S, în prezența de hidroxid de amoniu, hidroxizi conform ecuației generale :
2Me3+ + 3(NH4)2S + 6HOH → 2Me(OH)3 ↓ + 6NH4+ + 3H2S
în care Me3+ reprezintă unul din cei trei cationi trivalenți ai acestei subgrupe.
b) Subgrupa cationilor bivalenți: Fe2+, Co2+, Ni2+, Mn2+, Zn2+
Acești cationi formează cu reactivul grupei, sulfuri, conform ecuației generale :
Me2+ + (NH4)2S → MeS ↓ + 2NH4+
în care Me2+ reprezintă unul din cei cinci cationi ai acestei subgrupe.
Reactivul de grupă al acestor cationi este sulfura de amoniu la un pH = 9, creat prin adăugare de NH4Cl și NH4OH până la reacție alcalină (turnesol albastru), temperatura de 80-100 °C (la fierbere), concentrația reactivului : CNH3 = 1 mol/L, CS2- = 10-9 g/l.
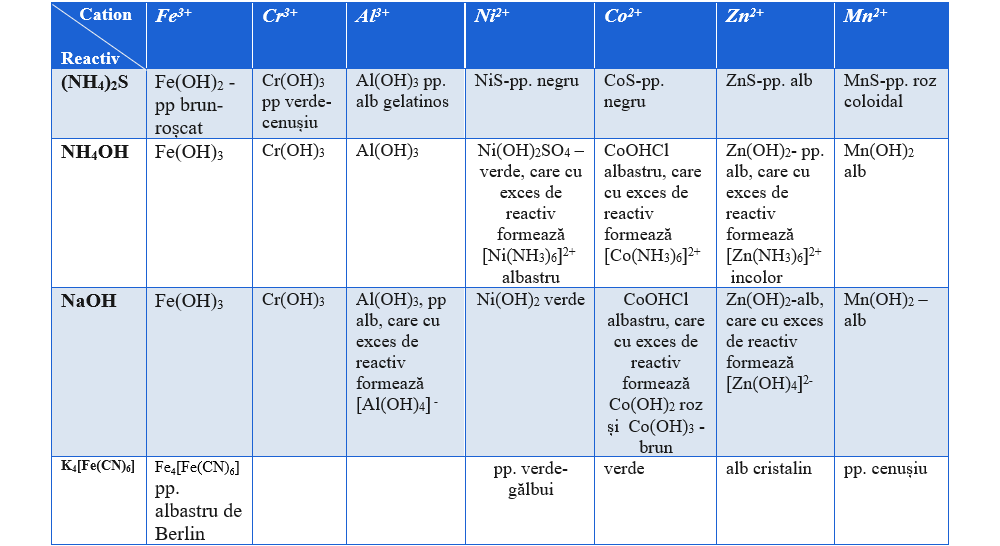
Tabel cu proprietățile chimice ale cationilor grupei a III-a analitice:*
👀 Experiment: Identificarea cationului de fier II (Fe2+) cu hidroxid de sodiu
🔥 Atenție! Hidroxidul de sodiu este caustic!
🔥 Atenție! Sulfatul de fier II este coroziv și periculos pentru mediu !
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de sulfat de fier II, soluție de hidroxid de sodiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeSO4 și adaugă soluție de hidroxid de sodiu până la precipitarea completă
- Ce observi ?
Se formează un precipitat alb-verzui de Fe(OH)2.
Concluzia experimentului:
Cationul Fe2+ formează cu hidroxidul de sodiu, un precipitat alb-verzui de hidroxid de fier (II) :
Fe2+ + 2OH- → Fe(OH)2 ↓
FeSO4 + 2NaOH → Fe(OH)2 ↓ + Na2SO4
Hidroxidul de fier (II), la aer, își schimbă repede culoarea de la verde până la roșu-brun.
👀 Experiment: Identificarea cationului de fier II (Fe2+) cu hexacianoferatul (III) de potasiu (fericianura de potasiu), K3[Fe(CN)6]
🔥 Atenție! Hexacianoferatul (III) de potasiu este periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de sulfat de fier II, fericianură de potasiu (cristale roșii), pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeSO4 și adaugă soluție de fericianură de potasiu până la precipitarea completă.
- Ce observi ?
Se formează un precipitat albastru de hexacianoferat (III) de fier (II).
Concluzia experimentului:
Cationul de fier II, Fe2+, formează cu hexacianoferatul (III) de potasiu (fericianura de potasiu) un precipitat de culoare albastră de hexacianoferat (III) de fier (II), cunoscut sub denumirea de 'albastru de Turnbull'.
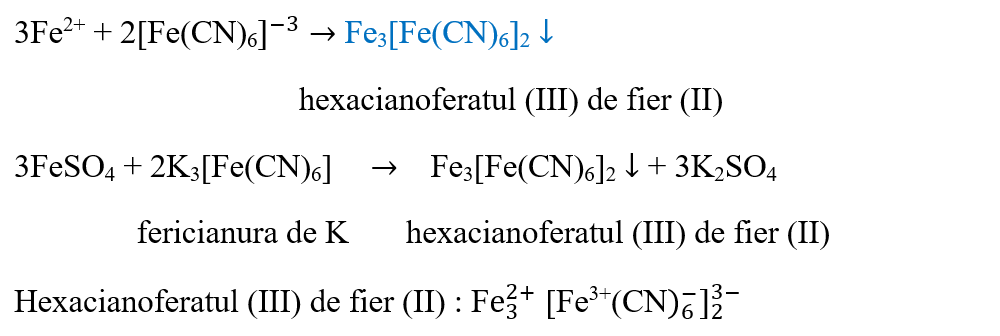
👀 Experiment: Identificarea cationului de fier III (Fe3+) cu hexacianoferat (II) de potasiu (ferocianura de potasiu), K4[Fe(CN)6]
🔥 Atenție! Hexacianoferatul (II) de potasiu este periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de fier III, soluție de hexacianoferat (II) de potasiu (ferocianura de potasiu), pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeCl3 și adaugă soluție de hexacianoferat (II) de potasiu până la precipitarea completă. Reacţia se poate executa pe lamă de microscop sau pe hârtie de filtru.
- Ce observi ?
Se formează un precipitat albastru de hexacianoferat (II) de fier (III).
Concluzia experimentului:
Hexacianoferatul (II) de potasiu, K4[Fe(CN)6] formează cu cationul de Fe3+, un precipitat albastru amorf de hexacianoferat (II) de fier (III), cunoscut sub denumirea de ��“albastru de Berlin” sau “albastru de Prusia”, folosit ca pigment.

👀 Experiment: Identificarea cationului de fier III (Fe3+) cu sulfocianură de potasiu (KSCN)
🔥 Atenție! Sulfocianura de potasiu de potasiu este nocivă, iritantă și periculoasă pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de fier III, soluție de sulfocianură de potasiu (KSCN), pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de FeCl3 și adaugă soluție de sulfocianura de potasiu.
- Ce observi ?
Se formează o soluție roșu- sângeriu, de sulfocianura ferică.
Concluzia experimentului:
Sulfocianura de potasiu (rodanura de potasiu), formează cu cationul de fier (III), o soluție roșu- sângeriu, de sulfocianura ferică:

👀 Experiment: Identificarea cationului de aluminiu (Al3+) cu hidroxid de sodiu
🔥 Atenție! Hidroxidul de sodiu este caustic!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de aluminiu, soluție de hidroxid de sodiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de AlCl3 și adaugă soluție de hidroxid de sodiu până la precipitare. Peste precipitatul alb de hidroxid de aluminiu adaugă soluție de NaOH până la dizolvarea sa.
- Ce observi ?
Se formează inițial un precipitat alb de hidroxid de aluminiu și după adăugarea în exces a NaOH se formează o soluție incoloră de hidroxoaluminat de sodiu.
Concluzia experimentului:
Cationul Al3+ cu hidroxidul de sodiu, formează hidroxidul de aluminiu, un precipitat alb gelatinos, solubil în exces de reactiv, cu formarea tetrahidroxoaluminatului de sodiu.

👀 Experiment: Identificarea cationului de cobalt II (Co2+) cu hexacianoferat (III) de potasiu
🔥 Atenție! Hexacianoferatul (III) de potasiu este toxic și periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de clorură de cobalt II, soluție de hexacianoferat (III) de potasiu, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de CoCl2 și adaugă soluție de hexacianoferat (III) de potasiu până la precipitarea completă.
- Ce observi ?
Se formează un precipitat verde de hexacianoferat (II) de cobalt (II).
Concluzia experimentului:
Hexacianoferatul (III) de potasiu (fericianura ce potasiu), K3[Fe(CN)6], formează cu cationul de Co2+, un precipitat verde de hexacianoferat (II) de cobalt (II).
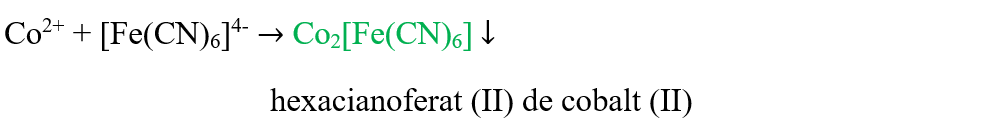
👀 Experiment: Identificarea cationului de nichel II (Ni2+) cu hidroxidul de amoniu
🔥 Atenție! Hidroxidul de amoniu (soluție diluată de amoniac) este iritant și periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de sulfat de nichel (II),soluție diluată de amoniac, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de NiSO4 și adaugă soluție de amoniac diluată până la precipitarea completă. Adaugă peste precipitatul verde soluție de amoniac (hidroxid de amoniu) până la dizolvarea sa.
- Ce observi ?
Se formează un precipitat verde și după adăugarea în exces a NH4OH devine o soluție albastru-deschis.
Concluzia experimentului:
O soluție diluată de amoniac, separă din soluții concentrate ale sărurilor de nichel, un precipitat de săruri bazice de culoare verde, solubile în exces de reactiv, cu formarea unui complex solubil, de culoare albastru deschis.
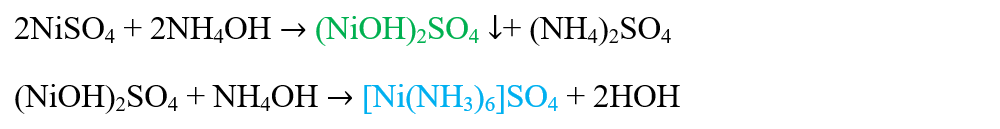
👀 Experiment: Identificarea cationului de zinc (Zn2+) cu hidroxidul de amoniu
🔥 Atenție! Hidroxidul de amoniu este iritant și periculos pentru mediu!
Materiale necesare:
Sticlă de ceas sau eprubetă, soluție de sulfat de zinc,soluție diluată de amoniac, pipetă.
Descrierea experimentului:
- Pune pe sticla de ceas câteva picături de soluție de ZnSO4 și adaugă soluție de amoniac diluată până la precipitarea completă. Adaugă peste precipitatul alb soluție de amoniac (hidroxid de amoniu) până la dizolvarea sa.
- Ce observi ?
Se formează inițial un precipitat alb și după adăugarea în exces a NH4OH devine o soluție incoloră.
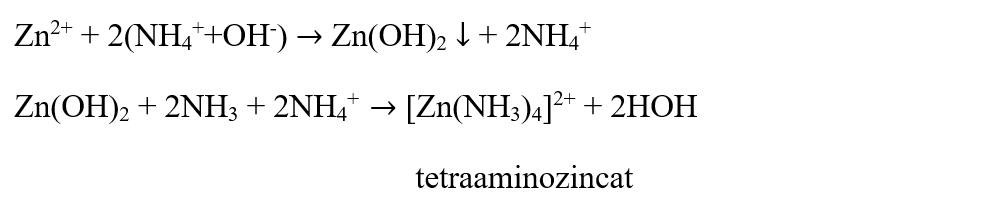
Concluzia experimentului:
Hidroxidul de amoniu formează cu cationul de Zn2+ hidroxidul de zinc, un precipitat alb gelatinos, solubil în exces de reactiv, în prezența sărurilor de amoniu, cu formarea unui complex solubil de tetraaminozincat.