VI.3. Legea lui Avogadro. Volum molar.
👀 Experiment: Numărul lui Avogadro și moli de molecule
Legea lui Avogadro:
Volume egale de gaze diferite, aflate în condiții identice de temperatură și presiune, conțin același număr de molecule.
Numărul lui Avogadro (NA) este o constantă universală și reprezintă numărul de particule (atomi, molecule, ioni pozitivi sau ioni negativi) ce se găsesc într-un mol de substanță.
Numărul de moli se notează cu litera grecească „niu” (υ) și se calculează cu relația:
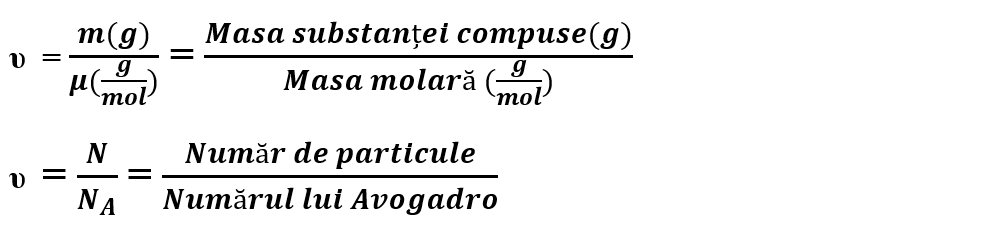
Numărul lui Avogadro = NA = 6,023 ∙ 1023 particule
Un mol din orice gaz ocupă în condiții normale de temperatură (0 °C) și presiune (1 atm) un volum, numit volum molar = Vμ = 22,4 L/mol
Numărul de moli:
