II.7.1. Reacția de halogenare prin reacții de substituție.
Reacția de halogenare este procesul chimic prin care se introduc în molecula unui compus organic unul sau mai mulţi atomi de halogen (F, Cl, Br, I).
Reacția de halogenare poate avea loc:
I. Prin reacții de substituție a atomilor de hidrogen dintr-o hidrocarbură cu atomi de halogen.
II. Prin reacții de adiție a halogenilor sau hidracizilor la hidrocarburi nesaturate.
Halogenarea prin reacții de substituție are loc după următoarea schema generală:
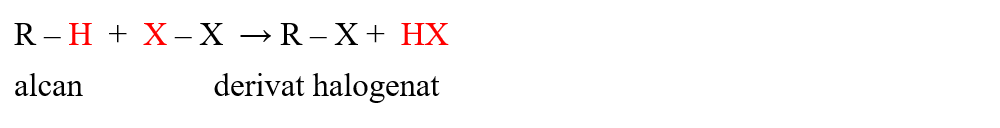
Exemple de reacții de halogenare prin reacții de substituție:
- Fabricarea freonului (diclordifluormetan), care este o reacţie de substituţie a atomilor de clor din tetraclorură de carbon cu atomii de fluor din acidul fluorhidric.
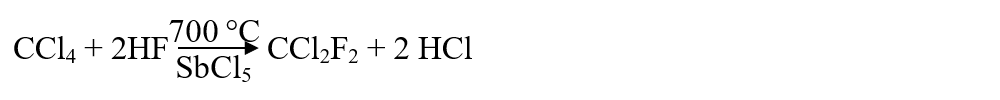
- Reacția de halogenare a metanului are loc în prezența luminii ultraviolete sau la temperatură (300-600 °C):

- Reacția de substituție la alcani este neorientată (poate fi substituit hidrogenul de la oricare atom de carbon), rezultând un amestec de izomeri monoclorurați.

🔦 Observații importante:
a) Determinările experimentale au arătat faptul că toate reacțiile de halogenare au ca produși de reacție un amestec al tuturor izomerilor posibili, ceea ce indică faptul că toți atomii de hidrogen din molecula alcanilor sunt susceptibili substituției. Totuși, amestecul cu produșii de reacție nu este un amestec statistic: atomii de hidrogen secundari și terțiari favorizează substituția, datorită stabilității mărite a radicalilor secundari și terțiari formați.
Reactivitatea atomilor de hidrogen legați de atomi de carbon crește de la atomul de C nular, primar, secundar, terțiar.

b) Clorul, fiind mai reactiv decât bromul, este mai puțin selectiv, formând un amestec de izomeri. Bromul mai puțin reactiv substituie atomii de hidrogen mai reactivi, fiind mai selectiv. Astfel, la monobromurarea butanului se obține un amestec de 2-bromobutan (halogenură secundară) în procent de 98% și 1-bromobutan (halogenură primară) în procent de 2%. În schimb, la monoclorurarea butanului se obține un amestec de 2-clorobutan (halogenură secundară) în procent de 67% și 1-clorobutan (halogenură primară) în procent de 33%.
În cazul monohalogenării neopentanului (2,2-dimetilpropan) se obține un singur compus monohalogenat:
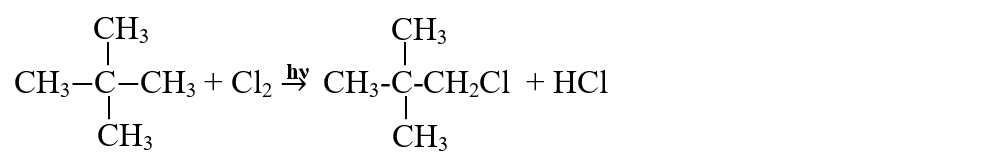
c) Compușii halogenați cu fluor și iod se obțin prin metode indirecte, din cauza reactivității prea mari a fluorului și prea reduse a iodului.
R-X + MeX́ → R-X́ + MeX, unde:
X = Cl, Br
X�́ = F, I
Me = metal
Exemple de reacții de halogenare prin reacții de substituție:
- Reacția de substituție la hidrocarburi aromatice
Reacția de halogenare a arenelor la nucleu are loc când un atom de H din nucleul aromatic este înlocuit de un atom de halogen, X (X = Cl, Br, I), cu formarea de derivați halogenați aromatici, Ar-X.
- Halogenarea benzenului se face în prezență de catalizatori: FeCl3, FeBr3, AlCl3 pentru Cl2 și Br2 și HNO3 pentru I2:

Clorobenzenul (clorura de benzil) este utilizat ca: diluant pentru uleiuri, grăsimi, rășini, cauciuc, etil-celuloză, bachelită, producerea de insecticide, coloranți, medicamente și substanțe aromatice.
- Halogenarea fenolului are loc mai ușor și cu o viteză mai mare comparativ cu benzenul, deoarece grupa hidroxil este un substituent de ordinul I, care activează nucleul aromatic.
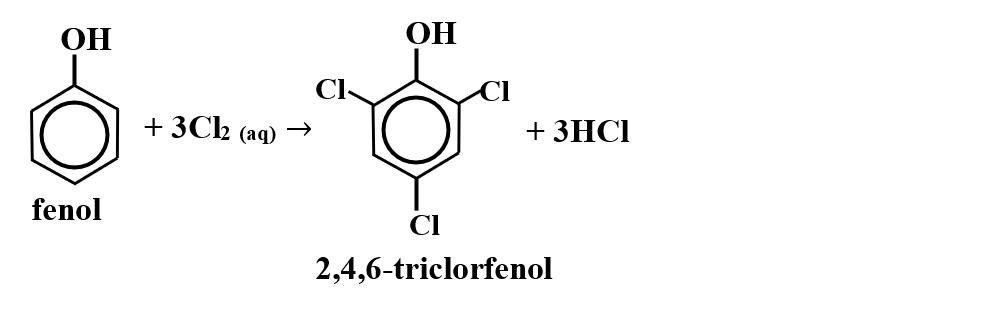
De exemplu, clorurarea fenolului se realizează cu catalizator de acid acetic, obținându-se 2,4,6-triclorfenol, folosit ca insecticid.
👀 Experiment: Reacția de bromurare a fenolului
Materiale necesare:
Pahar Berzelius, cristale de fenol, etanol, apă de brom, pipetă.
Descrierea experimentului:
- Dizolvă în pahar câteva cristale de fenol în 2 ml de etanol.
- În soluția de fenol adaugă apa de brom cu pipeta până la obținerea unui precipitat alb.

Concluzia experimentului:
Reacția de bromurare a fenolului are loc extrem de rapid, la temperatura camerei, fiind folosită la dozarea cantitativă a fenolului.
2,4,6-tribromfenol este folosit ca fungicid și pentru conservarea lemnului.