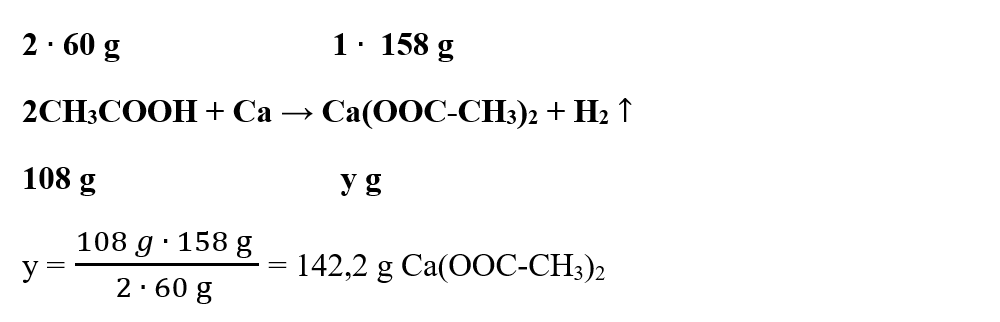III.2.9. Probleme rezolvate la acizi carboxilici.
🔓 Probleme rezolvate
1. Un acid monocarboxilic saturat cu formula generală C2H2nO2, conține 48,65% carbon. Determină formula moleculară și structurală a acidului.
Rezolvare:
Întrucât datele problemei sunt insuficiente pentru a determina formula acidului, vom lua pe rând fiecare acid monocarboxilic saturat.
a) Vom începe cu acidul metanoic (acidul formic) pentru a vedea ce procent de carbon conține:
Calculăm masa molară a acidului metanoic (HCOOH):
μCH2O2 = 1 ∙ AC + 2 ∙ AH + 2 ∙ AO = 1 ∙ 12 + 2 ∙ 1 + 2 ∙ 16 = 46 g/mol
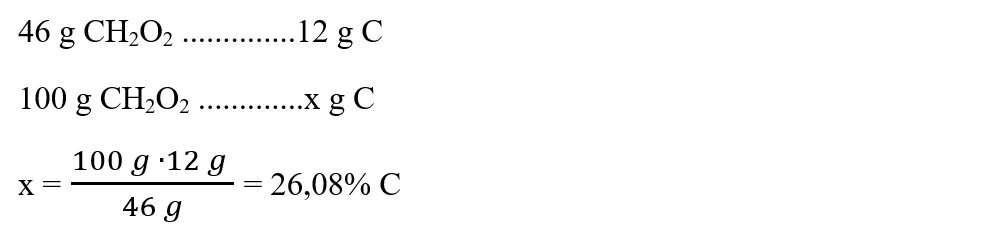
Deci, acidul metanoic nu este acidul căutat, care să conțină 48,65% C.
b) Continuăm cu acidul etanoic (acidul acetic) pentru a vedea ce procent de carbon conține:
Calculăm masa molară a acidului etanoic (CH3COOH):
μC2H4O2 = 2 ∙ AC + 4 ∙ AH + 2 ∙ AO = 2 ∙ 12 + 4 ∙ 1 + 2 ∙ 16 = 60 g/mol

Deci, acidul etanoic nu este acidul căutat, care să conțină 48,65% C.
c) Continuăm cu acidul propanoic pentru a vedea ce procent de carbon conține:
Calculăm masa molară a acidului propanoic (CH3CH2COOH):
μC3H6O2 = 3 ∙ AC + 6 ∙ AH + 2 ∙ AO = 3 ∙ 12 + 6 ∙ 1 + 2 ∙ 16 = 74 g/mol
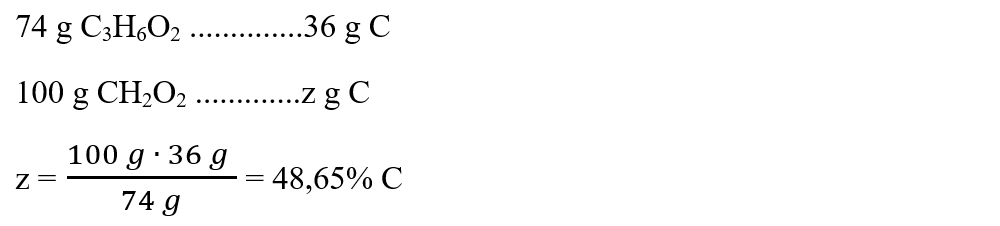
Deci, acidul propanoic este acidul căutat, care conține 48,65% C.
2. 172,5 g sol. 80% alcool etilic este supusă fermentației acetice. Știind că randamentul reacției de fermentație acetică este de 60% și că 50% din acidul acetic rezultat reacționează cu calciu, cu formarea acetatului de calciu, numit în medicină soluție Burow (folosit ca astringent prin contracția vaselor de sânge, ameliorând inflamația și mâncărimea pielii inflamate), determină:
a) Ce masă de acid acetic se obține ?
b) Ce masă de acetat de calciu se obține ?
Rezolvare :
a)
Calculăm masa de etanol din soluția dată cu regula de trei simplă:

Calculăm masa molară a etanolului și a acidului acetic:
μC2H5OH = 2 ∙ AC + 6 ∙ AH + 1 ∙ AO = 2 ∙ 12 + 6 ∙ 1 + 1 ∙ 16 = 46 g/mol
μCH3COOH = 2 ∙ AC + 4 ∙ AH + 2 ∙ AO = 2 ∙ 12 + 4 ∙ 1 + 2 ∙ 16 = 60 g/mol
Notăm datele problemei pe ecuația reacției chimice și aflăm masa teoretică a etanolului, conform ecuației chimice:

Calculăm masa practică a acidului acetic, aplicând formula randamentului unei reacții chimice:
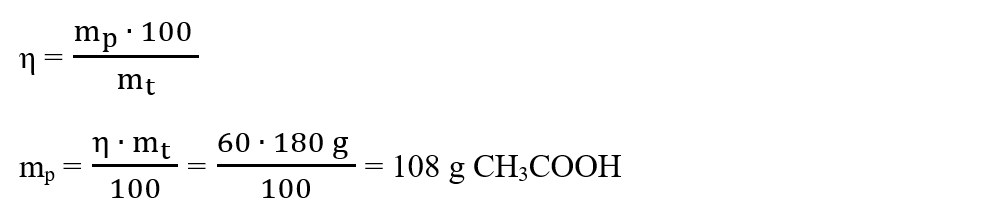
b)
Calculăm masa molară a acetatului de calciu:
μCa(OOC-CH3)2 = 1 ∙ ACa + 4 ∙ AO + 4 ∙ AC + 6 ∙ AH = 1 ∙ 40 + 4 ∙16 + 4 ∙ 12 + 6 ∙ 1= 158 g/mol
Notăm datele problemei pe ecuația reacției chimice dintre acidul acetic și calciu și aflăm masa acetatului de calciu obținut: