II.2.8. Exerciții și probleme rezolvate la alchene.
🔓 Exerciții și probleme rezolvate
1. Denumește conform IUPAC următoarele alchene:
a)

b)

Rezolvare:
a) Numerotăm atomii de C astfel încât să avem cea mai lungă catenă în care se află dubla legătură și atomul de carbon din dubla legătură să primească numărul cel mai mic.

b) Numerotăm atomii de C astfel încât să avem cea mai lungă catenă în care se află dubla legătură și atomul de carbon din dubla legătură să primească numărul cel mai mic.

2. Se dau următoarele formule moleculare: C4H6, C6H12, C5H12.
a) Precizează care dintre formulele moleculare corespund unor alchene.
b) Scrie formulele de structură ale tuturor izomerilor alchenelor respective, cu denumirea conform IUPAC.
Rezolvare:
a) Alchenele au formula generală CnH2n. Deci, numai C6H12 corespunde unei alchene.
b) Alchenele cu cel puțin 4 atomi de C în moleculă prezintă trei tipuri de izomerie: de catenă, de poziție, geometrică.
b.1. Izomerii de poziție a legăturii duble ai hexenei:

b.2. Izomerii de catenă ai hexenei sunt cu catenă liniară și cu catenă ramificată.
- 1-hexena (catenă liniară), 2-metil-1-pentena (catenă ramificată), 2,3-dimetil-1-butena (catenă ramificată):



- 2-hexena (catenă liniară), 2-metil-2-pentena (catenă ramificată), 2,3-dimetil-2-butena (catenă ramificată):



- 3-hexena are același izomeri de catenă cu 2-hexena.
b.3. Izomerii geometrici apar datorită împiedicării rotației libere în jurul dublei legături (planul legăturii π este perpendicular pe planul legăturii σ). Alchenele cu perechi identice de doi substituenți diferiți la fiecare dintre cei doi atomi ai legăturii duble au izomeri geometrici.
Numai 3-hexena are doi izomeri geometrici: cis-3-hexena (când substituenții identici sunt de aceeași parte) și trans-3-hexena (când substituenții identici sunt în părți opuse planului dublei legături).
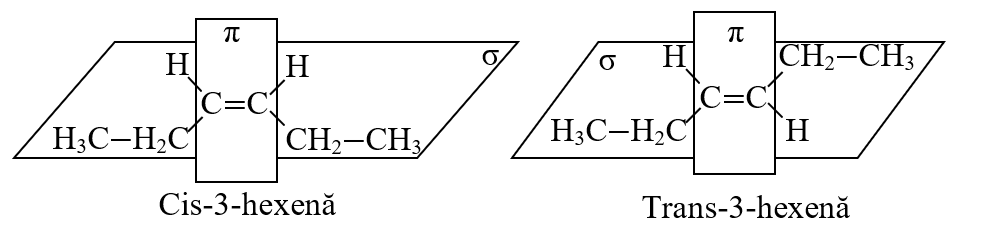
3. Calculează volumul de etenă de puritate 90%(procente volumice) necesar obținerii a 258 g de clorură de etil (kelen) cu un randament de 80%.
Rezolvare:
Scriem ecuația reacției de adiție a acidului clorhidric la etenă:

Din formula randamentului se calculează masa teoretică, mt, de clorură de etil (kelen) obținută:

Calculăm masa molară a kelenului:

Notăm datele problemei pe ecuația reacției chimice:
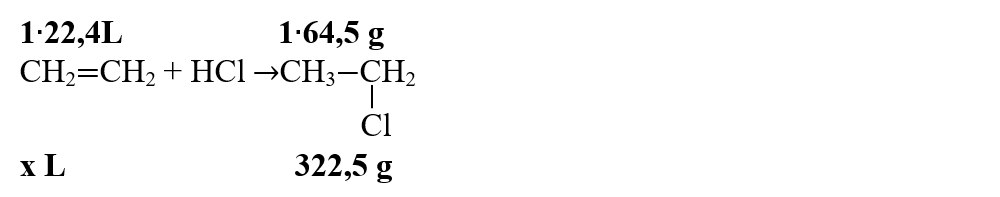
Din proporțiile astfel obținute, se calculează volumul de etenă consumat:
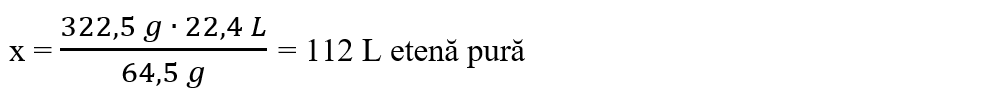
Se află volumul de etenă de puritate 90% cu regula de trei simplă:
